当前位置:首页 > 行业资料 > 纺织服装 > 有机化学第二章 饱和烃
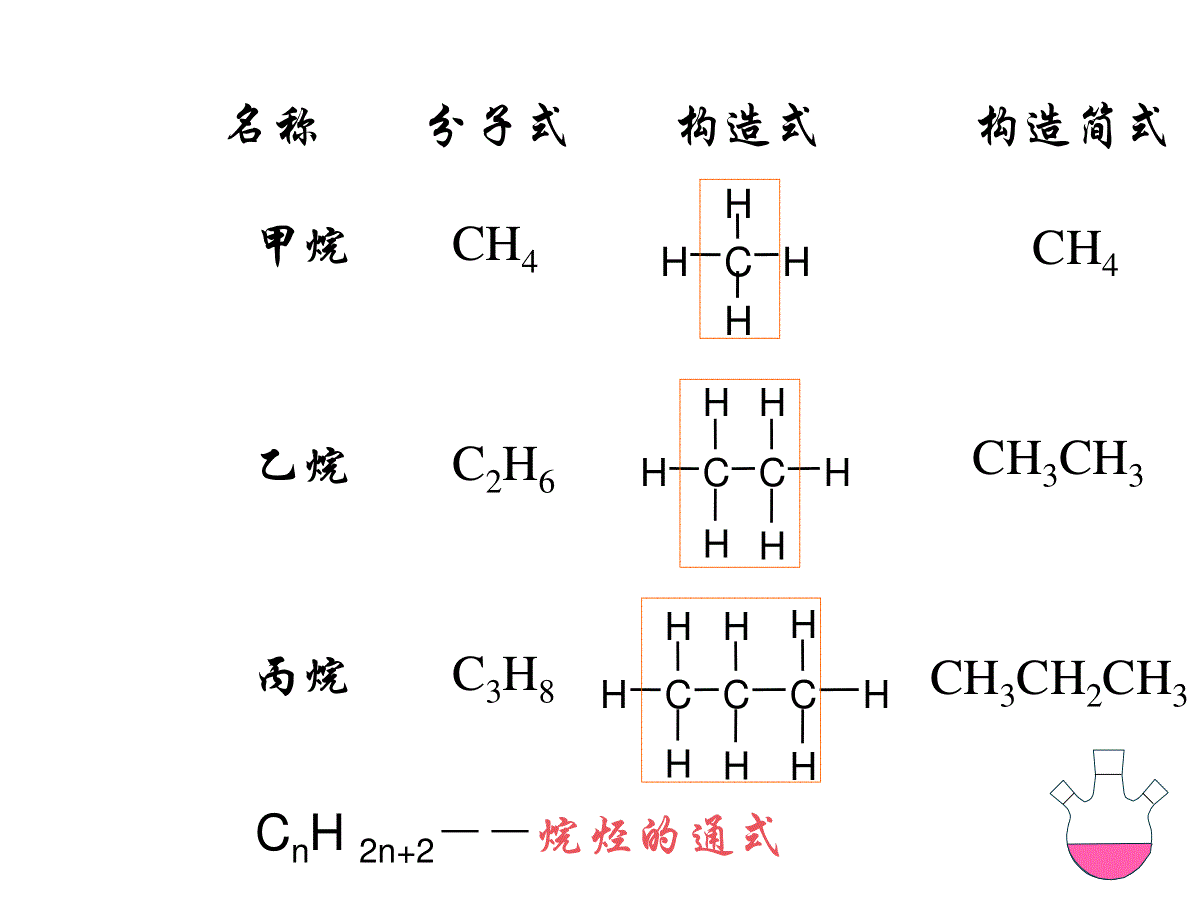
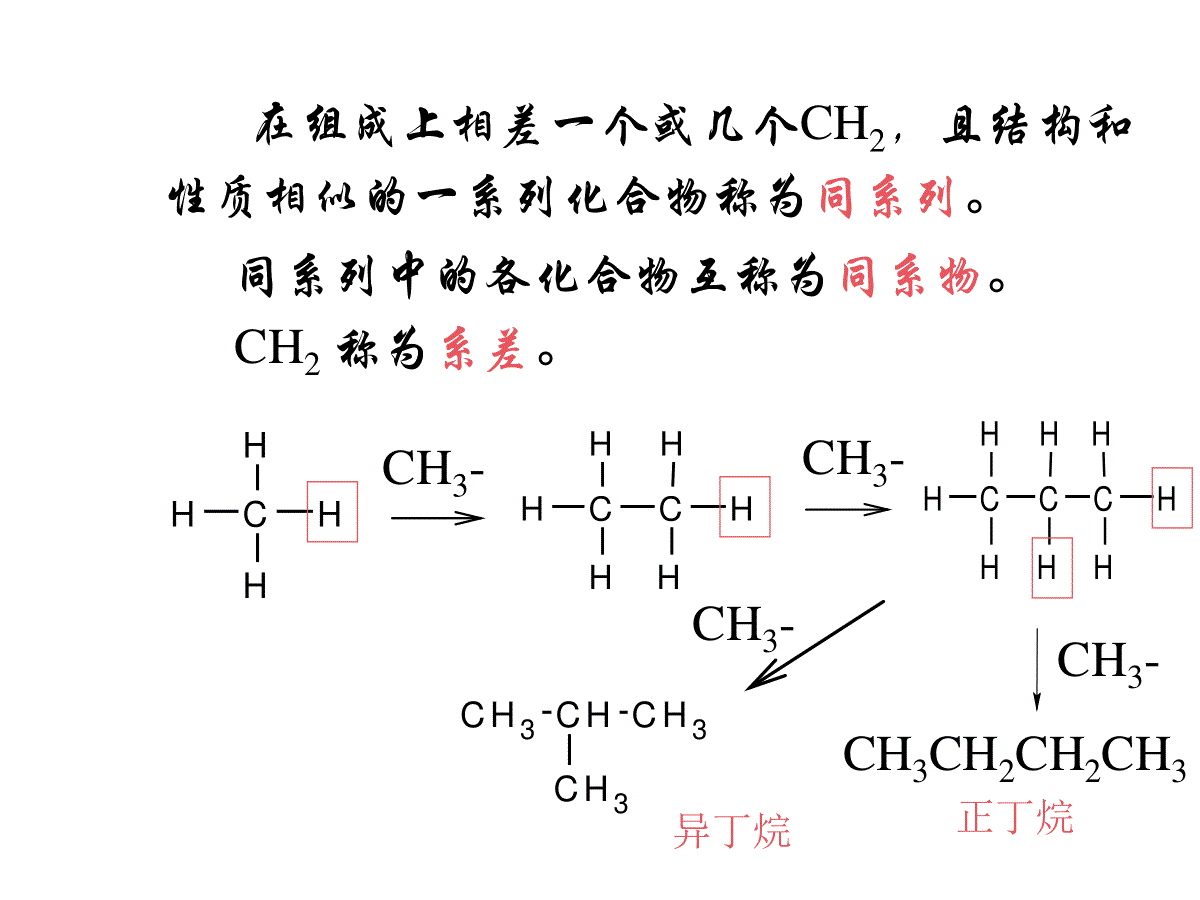
第二章烷烃第一节同系列和同分异构第二节命名第三节烷烃的结构第四节乙烷和丁烷的构象第五节物理性质第六节化学性质第七节自然界的烷烃习题12345678911023456789111234567891102345678911C、H化合物――烃hydrocarbon烃开链烃(脂肪烃)环烃饱和烃――烷烃不饱和烃――烯烃二烯烃炔烃脂环烃芳香烃1234567891102345678911第一节同系列和同分异构CHHHH名称分子式构造式构造简式甲烷CH4CH4乙烷C2H6CCHHHHHHCH3CH3丙烷C3H8CCHHHCHHHHHCH3CH2CH3CnH2n+2--烷烃的通式在组成上相差一个或几个CH2,且结构和性质相似的一系列化合物称为同系列。同系列中的各化合物互称为同系物。CH2称为系差。CHHHHCCHHHHHHCCHHHCHHHHHCH3-CH3-CH3CH2CH2CH3正丁烷CH3CHCH3CH3异丁烷CH3-CH3-回首页下一页上一页烷烃的同分异构体数目碳原子数异构体数目碳原子数异构体数目123451112367891059183575同分异构体:分子式相同,而结构和性质不同的化合物碳架异构:碳骨架不同引起的构造异构构造异构体:分子式相同,分子内原子间相互连接的次序不同回首页下一页上一页主链由长到短,支链由整到散,位置由心到边(末端碳除外),排布孪邻到间。例如:C6H14C-C-C-C-C-CH3H2H2H2H2H3CCCCCCHCCCCCCH3H3H2H2HH3CCCCCCH3H2H3H3H3CCCCCCH3HHH3H3H3H3H3H3H2H2同分异构体的写法回首页下一页上一页第二节命名一、伯、仲、叔、季碳原子及伯、仲、叔氢原子CH3CCHCH2CH3CH3CH3CH31°C2°C4°C3°C二、烷基CnH2n+1-R-CH3-甲基CH3CH2-乙基CH3CH2CH2-正丙基CH3CH-CH3异丙基•正烷基:去掉直链烷烃末端氢原子所得的原子团叫正烷基。命名时用“正”或“normal”的第一个字母“n”表示。•仲烷基:去掉一个仲氢原子所得烷基叫仲烷基。用“仲”或“secondary”的前三个字母“sec”表示。•叔烷基:去掉一个叔氢原子所得烷基叫叔烷基。用“tertiary”的前一个字母“t”表示。异烷基:链端倒数第二位碳原子上带有一个甲基支链。用“isomeric”的前一个字母“i”表示。回首页下一页上一页CH3CH2CH2CH2-CH3CH2CH-CH3CH3CHCH3CH2-CH3C-CH3CH3正丁基仲丁基异丁基叔丁基12345678911023456789111.习惯命名法甲、乙、丙、丁、戊、己、庚、辛、壬、癸为了区分同分异构体,通常采用一些词头来表示:正(n)——表示直链烷异(iso)——表示链端第二位C原子上带有一个甲基。新(neo)——表示链端第二位C原子上带有两个甲基CH3CH2CH2CH2CH3CH3CHCH2CH3CH3CCH3CH3CH3CCH2CH3CH3CH3正戊烷异戊烷新戊烷新己烷CH3H3C适用于简单的有机化合物三、烷烃的命名上一页下一页回首页下一页上一页(1)主链——最长碳链(2)编号——距支链最近端开始(3)取代基表示法——数目:二、三、四…次序:先小后大123456CH3CHCH2CHCH3CH2CH3CH2CH32-甲基-4-乙基已烷(4)多条最长碳链时,主链——取代基最多3CH3CH2CHCH2CH2CH3CHCHCH32-甲基-3-乙基已烷3-异丙基已烷2、系统命名法IUPAC╳回首页下一页上一页(5)在多条支链时,采取“最低系列”编号方法。3CH3CHCH2CH2CHCHCH3CH3CHCH32,3,6-三甲基庚烷2,5,6-三甲基庚烷╳50403020100CH3CH2CHCHCH2CH2CH2CH2CHCH3CH3CH3CH32,7,8—三甲基癸烷CHCHCH3CHCH2CH2CHCH3CH3CH3CH3H2CH3C2,3,5—三甲基—4—丙基庚烷练习:sp3杂化碳原子形成的甲烷sp3杂化碳原子形成的乙烷六个C—Hσ键和一个C—Cσ键四个C—Hσ键第三节烷烃的结构在甲烷分于中,已知碳原子为sp3杂化,C—Hσ键是由碳原子的sp3杂化轨道与氢原子的1s轨道在对称轴的方向交盖而成。CH3-CH3σ键的特性:a、σ键存在于任何含有共价键的有机分子中,且在分子中可以单独存在。b、由于σ键是在成键轨道方向的直线上相互交盖而成,故交盖程度大,σ键的键能较大,可极化性较小。C、σ键可以沿键轴自由旋转而不被破坏。H2CCH3CH3109.5°丙烷分子中碳碳间的σ键其他烷烃上碳原子所连接的四个原子或原子团并不完全相同,因此每个碳上的键角并不完全相同。除乙烷外,烷烃分子的碳链并不排布在同一条直线上,而是曲折地排布在空间。为了书写的方便,碳链仍然写成直链的形式。也可用键线式来书写烷烃的分子结构。用锯齿型线的角及其端点来代表碳原子,除氢原子外的其他原子或原子团必须写出。CH3CH2CH2CH2CHCH2CH2CHCH2CH2COOHCIOHCOOHOHCI1234567891011第四节乙烷、丁烷的构象构象:由于围绕单键旋转而引起的分子中各原子在空间的不同排列方式称为构象。一.乙烷的构象乙烷的的构象是无穷多的,其中有典型意义的两种构象是重叠式和交叉式的构象乙烷分子绕C-C单键360o时要经过三个重叠式和三个交叉式构象。这两种构象可分别用透视式和纽曼(M.S.Newman)投影式表示:Newman投影式:是从C—Cσ键的延长线上观察,两个碳原子在投影式中处于重叠位置。表示距离观察者较近的碳原子及其三键。表示距离观察者较远的碳原子及其三个键。每一个碳原子所连接的三个键,在投影式中互呈120°角。HHHHHHHHHHHH1.重叠式构象中,两个碳原子上的H原子相互重叠,无论C-H键上的σ电子对之间,或H原子之间的距离均最近,相互排斥力最大,因此能量最高,是最不稳定的构象2.在交叉式构象中,两个H原子相互交错,无论C-H键上的б电子对之间,间或H原子之间的距离均最远,相互排斥力最小,因此能量最低,是最稳定的构象3.重叠式的能量比交叉式能量约高12.6kj/mol,这种能量差叫做能垒。单键的旋转并不是完全自由的,但是在室温下,分子热运动即可越过此能垒,而使各种构象迅速互变,所以在室温下乙烷是无数构象组成的平衡混合物二.丁烷的构象CH3CH2-CH2CH3沿C2-C3σ键旋转产生四个极限构象:丁烷四种典型构象的能量高低为:对位交叉式<邻位交叉式<部分重叠式<全重叠式第五节物理性质一、物态在室温下,C1-C4气体;C5-C16液体;C17以上为固体。二、沸点(b.p.)蒸气压与分子间作用力有关分子间作用力越大,沸点越高M↑,b.p↑;支链↑,b.p↓三、熔点烷烃熔点较低1、M↑,m.p.↑2、同分异构体:对称性越大,熔点越高。3、含偶数C,m.p↑的多;含奇数C,m.p↑的少从而形成了“偶上奇下”两条曲线。五、溶解度“相似相溶”规则,难溶于水,易溶于有机溶剂四、密度所有烷烃密度小于1,M↑,d↑,最后接近于0.8左右CH3CH2CH2CH2CH3CH3CHCH2CH3CH3CH3CCH3CH3CH3正戊烷异戊烷新戊烷b.p.(℃)36.127.99.5m.p.(℃)-129.8-159.9-16.81.氧化反应烷烃在空气中点火引发可发生燃烧反应,并放出大量的热。在催化剂(KMnO4,MnO2或脂肪酸锰盐)存在下,烷烃可以氧化为高级脂肪酸。所得产物为混合物,工业上应用价值不大。RCH2-CH2R’+O2RCOOH+R’COOH催化剂2.取代反应烷烃分子中的氢原子被其他原子或基团取代的反应,称为取代反应。通过自由基取代分子中氢原子的反应,称为自由基取代反应。被卤素取代的反应叫卤代反应,也称为卤化反应。(1)甲烷的氯代反应CH4+Cl2光或高温CH3Cl+CH2Cl2+CHCl3+CCl4+ClH产物:四种氯代化合物的混合物影响产物组成的因素:(1)反应物的摩尔比(2)反应时间过量存在的甲烷比一氯甲烷更容易与氯反应甲烷和氯在强光下发生猛烈的反应,甚至发生爆炸。(2)其他烷烃的氯代反应——伯、仲、叔氢的活泼性CH3CH3+Cl2CH3CH2Cl+ClHhvCH3CHCl2+Cl2CH3CH2Cl+hvCH2CH2ClCl乙烷:丙烷:+Cl2CH3CH2CH3+光CH3CH2CH2ClCH3CHCH3Cl1°H2°H6个2个以1°H的反应活性为1活性:1xⅠ()CH3CH2CH2CH3+Cl2hν取代1H。取代2H。CH3CH2CH2CH2ClCH3CHCH2CH3Cl正丁基氯仲丁基氯28%72%Ⅱ()CH3CHCH3CH3+Cl2取代1H。取代3H。CH3CHCH2ClCH3CH3CHCH3CH3Cl异丁基氯叔丁基氯64%36%hνⅠ()72(仲丁基氯)28(正丁基氯)=2H数目。2H活性。1H数目。1H活性。=42H活性。612H活性。=722864=3.86Ⅱ()36(叔丁基氯)64(异丁基氯)=13H活性。913H数目。3H活性。1H数目。1H活性。=3H活性。=366491=5.06CH3HCH3+HCH2HCH3CH3CH2+HCH3CHHCH3+HCH3CHCH3CH3CHCH3CH3CH3CCH3CH3+Hmol-1410.3439.6KJmol-1KJ397.7mol-1KJ389.4mol-1KJ离解能,反应活性。烷烃分子中伯、仲、叔氢原子活泼性的不同,也可用键的离解能不同来解释:H原子的反应活性次序为:3°H>2°H>1°H,显然,自由基形成的难易应为:3。2。1。CCCCH3易难容易形成的自由基,一定是稳定的自由基。∴自由基的稳定性顺序为:。2。1。CCCCH33反应活性:FClBrI(3)烷烃与其他卤素的取代反应烷烃与氟作用时,反应剧烈并有大量热放出,反应不易控制,有时会引起爆炸,因此烷烃氟代并无实用价值;烷烃不能与碘反应,碘代烷必须用其它方法来制备。溴的活泼性不如氯,与烷烃反应比较缓慢,但溴更有选择性,溴尽量取代叔氢原子或仲氢原子,溴代反应更有用。正丁基氯仲丁基氯正丁基溴仲丁基溴28%72%2%98%CH3CH2CH2CH3Cl2hvhvBr2异丁基氯叔异丁基溴叔丁基溴丁基氯64%36%1%99%CH3CHCH3CH3Cl2hvBr2hv卤素的反应活性:Cl2Br2卤素的选择性:Cl2Br2(4)甲烷氯代反应历程在光照或高温下,烷烃的氯代反应属自由基链反应或自由基反应。甲烷反应历程如下:链引发:Cl:ClhνClCl+链增长:Cl+CH3HHCl+CH3CH3+Cl2CH3Cl+ClCH3Cl+ClHCl+CH2ClCH2Cl+Cl2CH2Cl2Cl+生成活泼质点原有的活泼质点消失,生成新的活泼质点。第七节自然界的烷烃烷烃的主要来源:石油和天然气从油田开采出来未经加工的石油叫原油,原油的主要成分是烃类(烷烃、环烷烃、芳香烃)原油,根据沸点的不同可以分馏得到不同的馏分:汽油、煤油、柴油、润滑油、石蜡、凡士林、沥青等天然气是蕴藏在地层内的可燃气体,甲烷含量不同,可分干天然气(含甲烷86%~99%)和湿天燃气(含甲烷60%~70%)可燃冰可燃冰的学名为“天然气水合物”,是天然气在0℃和30个大气压的作用下结晶而成的“冰块”。“冰块”里甲烷占80%~99.9%,可直接点燃,燃烧后几乎不产生任何残渣,污染比煤、石油、天然气都要小得多。西方学者称其为“21世纪能源”或“未来能源”。1立方米可燃冰可转化为164立方米的天然气和0.8立方米的水。科学家估计,海底可燃冰分布的范围约4000万平方公里,占海洋总面积的10%,海底可燃冰的储量够人类使用1000年。习题P28-29:2.3;2.5;2.9;2.11;2.13;2.16



 三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
本文标题:有机化学第二章 饱和烃
链接地址:https://www.777doc.com/doc-3317962 .html