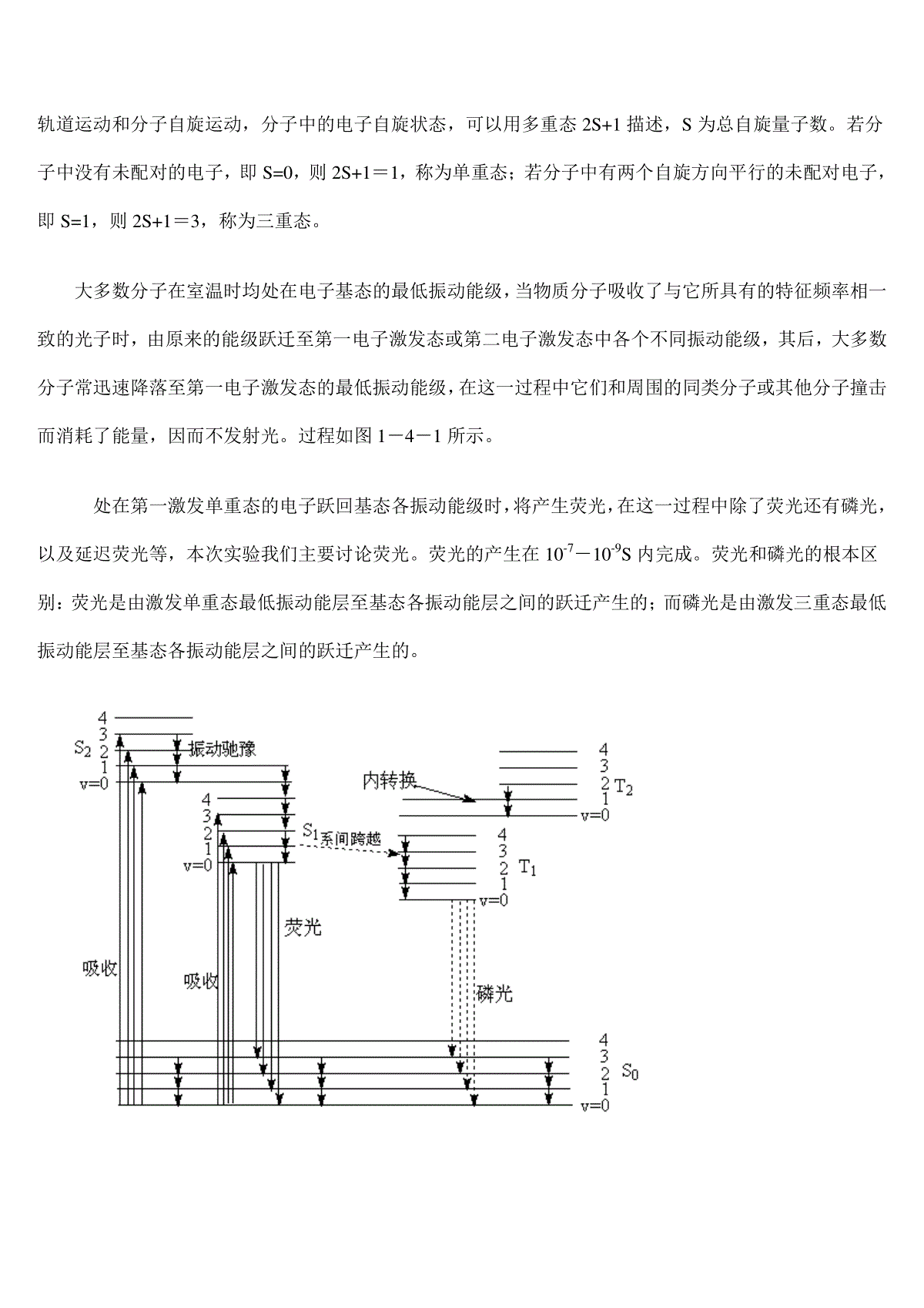
实验1-4荧光谱测量发布时间:2008-06-23实验1-4荧光谱测量某些物质受到电磁辐射而激发时,它们能重新发射出相同或较长波长的光。这种现象称为光致发光,荧光是光致发光现象中最常见的类型。如果停止照射,则荧光很快(10-6s)地消失。通常所观察到的荧光现象是指物质吸收了波长较短的紫外光后发出波长较长的可见荧光。实际上,荧光现象并不限于上述情况。有些物质吸收了紫外光,仍然发出波长稍长的紫外荧光。有些物质吸收了比紫外光波长短得多的X射线,然后发出波长比所吸收的X射线的波长稍长的X射线荧光,据此而建立了X射线荧光分析法。通过测量荧光的强度,可用于定量测定许多无机和有机物质,它已成为一种很有用的分析方法,特别在生物化学方面有着广泛的应用。通过实验学习和掌握荧光光度计测定物质荧光光谱的原理和方法;熟悉荧光分光光度计的结构及使用方法;测量物质的荧光光谱一、实验原理发光物质因引起发光的原因不同可分为:热致发光、光致发光、电场致发光、阴极射线发光、高能粒子发光及生物发光等多种发光方式。光致发光的原理是分子在吸收了光能后,从基能态跃迁到高能态,在它们再从高能态返回基能态时,以光能的形式向外释放之前吸收的外来能量,即光致发光所发生的光。(一)荧光的产生物质吸收光能后所产生的光辐射称之为荧光和磷光单重态和三重态。分子中的电子运动包括分子轨道运动和分子自旋运动,分子中的电子自旋状态,可以用多重态2S+1描述,S为总自旋量子数。若分子中没有未配对的电子,即S=0,则2S+1=1,称为单重态;若分子中有两个自旋方向平行的未配对电子,即S=1,则2S+1=3,称为三重态。大多数分子在室温时均处在电子基态的最低振动能级,当物质分子吸收了与它所具有的特征频率相一致的光子时,由原来的能级跃迁至第一电子激发态或第二电子激发态中各个不同振动能级,其后,大多数分子常迅速降落至第一电子激发态的最低振动能级,在这一过程中它们和周围的同类分子或其他分子撞击而消耗了能量,因而不发射光。过程如图1-4-1所示。处在第一激发单重态的电子跃回基态各振动能级时,将产生荧光,在这一过程中除了荧光还有磷光,以及延迟荧光等,本次实验我们主要讨论荧光。荧光的产生在10-7-10-9S内完成。荧光和磷光的根本区别:荧光是由激发单重态最低振动能层至基态各振动能层之间的跃迁产生的;而磷光是由激发三重态最低振动能层至基态各振动能层之间的跃迁产生的。图1-4-1荧光光谱能级跃迁示意图产生荧光的第一个必要条件是该物质的分子必须具有能吸收激发光的结构,通常是共轭双键结构;第二个条件是该分子必须具有一定程度的荧光效率。所谓荧光效率是荧光物质吸光后所发射的荧光量子数与吸收的激发光的量子数的比值。(二)荧光光谱荧光光谱:荧光光谱包括激发谱和发射谱两种。激发谱是荧光物质在不同波长的激发光作用下测得的某一波长处的荧光强度的变化情况,也就是不同波长的激发光的相对效率;发射谱则是某一固定波长的激发光作用下荧光强度在不同波长处的分布情况,也就是荧光中不同波长的光成分的相对强度。既然然激发谱是表示某种荧光物质在不同波长的激发光作用下所测得的同一波长下荧光强度的变化,而荧光的产生又与吸收有关,因此激发谱和吸收谱极为相似。但是激发光谱和吸收光谱不同,后者只说明材料的吸收,至于吸收后是否发完,就不一定了,因此将激发光谱与吸收光谱进行比较,可以判断哪种吸收对发光有用。由于激发态和基态有相似的振动能级分布,而且从基态的最低振动能级跃迁到第一电子激发态各振动能级的几率与由第一电子激发态的最低振动能级跃迁到基态各振动能级的几率也相近,因此吸收谱与发射谱呈镜象对称关系。(三)有稀土离子的激光晶体的荧光谱稀土离子激活的发光晶体在现代科学技术中有着广泛的应用。许多发光粉、上转换材料及激光材料就是掺稀土离子的。三价自由稀土离子的4f组态的电子波函数具有相同的宇称,没有电偶极辐射和吸收。当三价稀土离子进入晶体后,看到了发光。对此有人解释为:静态晶体场引起相反宇称的组态混杂,并由此观点出发推导了跃迁几率表达式。因为,跃迁几率决定光谱线的强度,两个能级之间的跃迁几率,跃迁截面(吸收或发射截面),辐射寿命,荧光强度,荧光分支比,量子效率等,这些标志强度的参数都是十分重要的发光参数。但是它们的实际测量有时候不是很容易。如果能够计算出跃迁几率,这些参数就可以得到了。现在以能级寿命为例进行简单的演绎说明。设能级E2上的离子数为N2,由于自发辐射N2将随着时间减少。设时间dt内N2的改变量为dN2,则:dN2=-A21N2dt或dN2/N2=-A21dt(1-4-1)积分后:N2=N20exp(-A21t)(1-4-2)N20为t=0时候的N2值。上式表明N2减少的快慢与几率系数A21的大小有关,A21越大,则N2减少越快。A21具有时间倒数的量纲,它的倒数为:所以上式可以改写为:(1-4-3)τ反映了粒子平均来说在能级E2上停留时间的长短,它叫做粒子在该能级上的平均寿命,τ也可理解为在能级E2上的粒子数减少到开始的1/e,所经历的时间。各种原子的各个能级的寿命τ与原子的结构有关,一般激发态能级的寿命数据级别为10-8S,也有一些激发态的能级寿命特别长的,可达到10-3S甚至1S,这种寿命特别长的叫做亚稳态。在激光晶体中,压稳态在激光的产生过程中起着特殊的作用。以上所讲只是与自发跃迁过程中对应的寿命,更确切的讲应叫能级的自然寿命。实际上由于原子间的碰撞或者其它外界干扰。都会使原子的跃迁几率大大增加,从而能级的实际寿命一般比自然寿命小几个数量级。二、实验配置进行分子荧光光谱分析的仪器称荧光分光光度计。它由5部分组成:光源;单色器;样品池;检测器;显示装置。WGY—10型荧光分光光度计的光路图如图1-4-2所示:光源:荧光分光光度计多采用氙灯作为光源,因它具有从短波紫外线到近红外线的基本上连续的光谱,以及性能稳定、寿命长等优点。近年来激光荧光分析应用日广,它采用激光器作为光源。单色器:是从复合光色散出窄波带宽度光束的装置,由狭缝、镜子和色散元件组成。色散元件包括棱镜和光栅。荧光分光光度计有两个单色器:激发单色器和发射单色器。图1-4-2荧光分光光度计的光路图试样容器:也称样品池,用于放置样品。光源、试样容器和探测器通常排成直角形,对于不透明的固体试样,则排成锐角形。检测器:通常采用光电倍增管作为检测器。显示装置:荧光分光光度计大多配有微处理机,其信号经处理后在屏上显示,并输给记录器记录。某些型号的荧光分光光度计,按下电键即可得出三维荧光光谱。荧光分光光度计可分为单光束与双光束两种。在单光束荧光分光光度计中,光源发出的光经激发单色器单色化的光只有一束,照射在样品池上,样品发出的荧光经过发射单色器色散后照射在光电倍增管上。三、实验内容与步骤(一)实验步骤1、将荧光分光光度开机,预热10分钟左右,将样品放入样品池中,测量激发谱。(具体软件操作见说明书)2、根据测得的激发谱,确定样品的激发波长,用此波长测量样品的发射谱。(二)实验内容1、利用下面给定的公式,结合荧光发射谱,对下图中的几条辐射进行相关计算。(1-4-4)(1-4-5)图1-4-3实际钕离子系统的跃迁能级示意图(1-4-6)(1-4-7)式中是自发辐射总跃迁几率,是能级寿命,是荧光分支比,是积分发射截面。λ是中心波长,e为电子电荷,n为折射率,h为普朗克常数,m是电子质量。思考题:1、荧光谱与磷光谱有什么不同与相同?2、荧光谱在分析物质特性是有什么用处?3、激发谱和发射谱有什么不同之处?




 三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
三七文档所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
本文标题:荧光光谱的相关概念
链接地址:https://www.777doc.com/doc-2057734 .html